Bệnh nang thận có thể gặp ở 50% dân số nhưng thường thầm lặng và được phát hiện tình cờ qua các xét nghiệm hình ảnh hoặc sau khi tử thiết.
Trong nghiên cứu bởi Terada và cộng sự (2008) 61 bệnh nhân có nang thận đơn giản và theo dõi trung bình 10 năm, các tác giả lưu ý rằng các nang tăng cả về kích thước và số lượng theo thời gian. Mức tăng trung bình là 1,9 mm mỗi năm. Điều thú vị là có hai nang phát triển thành ung thư trong quá trình nghiên cứu và không ghi nhận sự khác biệt về lâm sàng với các bướu lành tính khác. Các yếu tố nguy cơ cho sự phát triển của nang gồm: tuổi, nam giới, tăng huyết áp, suy thận (Terada và cộng sự , 2004).
Nang thận là tổn thương thận lành tính thường gặp nhất, chiếm hơn 70% các khối ở thận không có triệu chứng. Các nang có thể đơn độc hay nhiều nang, 1 bên hoặc 2 bên thận (Terada và cộng sự, 2002).
Nang thận có thể gây ra các triệu chứng như: đau hoặc cảm giác nặng vùng hông lưng, cao huyết áp, tiểu máu, nhiễm trùng, chèn ép gây bế tắc đường tiết niệu trên.
Nang thận có thể được khảo sát bằng siêu âm, CT hoặc MRI. Trên siêu âm, nang thận đơn giản có thành trơn láng, dịch bên trong không phản âm. Nếu có phản âm, vôi hóa, nốt, hoặc vách trong nang qua siêu âm là những nang phức tạp và cần được khảo sát bằng hình ảnh học có tiêm thuốc cản quang (Quaia et al, 2008 ; Eknoyan , 2009).
Phân loại Bosniak là phương pháp hữu ích nhất trong việc khảo sát các nang thận (Israel và Bosniak năm 2005; Warren và McFarlane, 2005). Nhìn chung, Bosniak type I, II, và IIF thường là lành tính, do đó không cần điều trị, cần theo dõi bằng hình ảnh học.
| Phân loại Bosniak | Hình ảnh học | Tỉ lệ ung thư | Điều trị |
| I | Nang đơn giản, vách mỏng không vôi hóa, dịch trong nang mật độ nước, không bắt thuốc cản quang. | 1.7% | Không điều trị, theo dõi |
| II | Có thể có vài vách mỏng và ít vôi hóa trên thành hoặc vách. Tổn thương đồng dạng <3cm (còn gọi là bướu nang mật độ cao) giới hạn rõ và bắt thuốc cản quang. | 18.5% | Không điều trị, theo dõi |
| IIF | Có thể chứa nhiều nốt vôi hoá, vách mỏng, thành hoặc vách dày. Không bắt thuốc cản quang, bờ giới hạn rõ. Tổn thương ≥ 3 cm cũng được xếp vào loại này. | 18.5% | Chụp lại để theo dõi kích thước |
| III | Thành và vách nang dày không đều, khó xác định. Tăng cản quang | 33% | Cắt bỏ |
| IV | Nang gần như ác tính, gồm loại III + tăng cản quang mô mềm. | 92.5% | Cắt bỏ |
Vì loại III và IV nguy cơ ác tính cao nên cần được điều trị phẫu thuật cắt bỏ. Đại đa số bướu nang đơn giản thường không cần tiếp tục theo dõi hoặc điều trị (Eknoyan, 2009). Nang lành tính hiếm khi to lên gây đau hoặc tăng huyết áp (Porpiglia et al, 2009; Zerem et al, 2009). Triệu chứng này cũng có thể xảy ra do hậu quả của xuất huyết trong nang tự phát hoặc chấn thương làm vỡ nang (Hughes và cộng sự, 1995; Rainio et al, 2006; Ishikawa và cộng sự, 2008; Vaidyanathan và cộng sự, 2008). Đối với các trường hợp nang thận có kích thước lớn và có triệu chứng thì có chỉ định can thiệp bằng cách chọc hút nang thận dưới hướng dẫn siêu âm và chích xơ bằng ethnol 95 độ hoặc cắt bỏ chỏm nang qua phẫu thuật nội soi. Do nang gần với các cấu trúc quan trọng của thận , nên nội soi là phương pháp tiếp cận an toàn và hiệu quả (Okumura và cộng sự, 2003; Camargo và cộng sự, 2005).

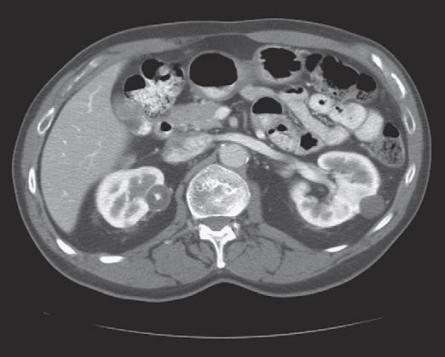
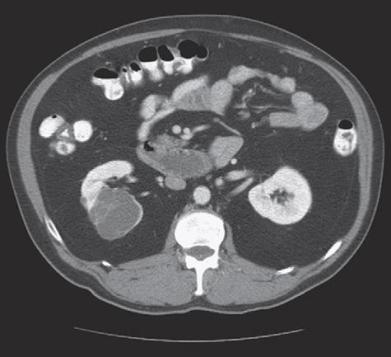
| A | B | C |
Hình 1. A: nang thận Bosniak I. B: nang thận Bosniak II, có vôi hóa bên trong. C:
nang thận Bosniak IIF, có vài vách mỏng trong nang (Copyright 2009, C.G. Wood.)
- BƯỚU TUYẾN VỎ THẬN (RENAL CORTICAL ADENOMA)
Bướu tuyến vỏ thận vẫn còn là một đề tài tranh cãi trong tiết niệu. Tỉ lệ mắc bướu tuyến vỏ thận tăng theo độ tuổi và giới tính nam, và những khối bướu này cũng có liên quan đến nang thận ở những bệnh nhân suy thận mạn giai đoạn cuối (Leroy và cộng sự, 2001; Denton và cộng sự, 2002; Snyder et al, 2006; Ferda và cộng sự, 2007). Bướu thường nhỏ, nằm ở phần ngoài vỏ thận và có hình nhú về mô học. Phần lớn không có triệu chứng lâm sàng và chỉ được phát hiện lúc mổ tử thi hay trên thận được cắt bỏ vì nguyên nhân khác.Tỉ lệ mắc bướu tuyến vỏ thận trong khám nghiệm tử thi khoảng 7% đến 23% (Licht, 1995 ; Renshaw, 2002 ; Minor et al, 2003). Trước đó Bell (1950) nhận thấy qua giải phẫu tử thi thì các bướu dưới 3cm ít gây di căn, trong khi các bướu lớn hơn 3cm lại có di căn nhiều hơn.
Bướu tuyến vỏ thận có thể có mối liên quan sinh học với sự phát triển của RCC và có khả năng hoá ác.
Đại đa số bướu tuyến vỏ thận không triệu chứng, và thường không thể phát hiện qua hình ảnh học do kích thước nhỏ (<1 cm), và không cần điều trị thêm. Chẩn đoán bướu tuyến vỏ thận vẫn còn gây tranh cãi, nhiều người tin rằng tất cả chúng có nguồn gốc từ biểu mô thận đặc có tiềm năng ác tính, do đó cần điều trị (Renshaw, 2002).
BƯỚU TUYẾN TRUNG THẬN (METANEPHRIC ADENOMA):
Bướu tuyến trung thận mới được mô tả gần đây, là bướu lành tính hiếm mà hình ảnh học thường khó phân biệt được với RCC. Bướu thường được tìm thấy tình cờ, ở nữ, khoảng 50-60 tuổi.
Chẩn đoán xác định bằng kết quả giải phẫu bệnh sau phẫu thuật cắt bướu.

Hình 2.CT scan bướu tuyến trung thận của một bệnh nhân nữ trung niên
ONCOCYTOMA
Oncocytoma thận là bướu lành tính thường gặp nhất xuất hiện như một khối tăng cản quang trên hình ảnh cắt ngang và được xem là RCC cho đến khi có kết quả giải phẫu bệnh sau mổ cắt bướu. Đây là một trong những thách thức trong chẩn đoán trước phẫu thuật cho các bác sĩ niệu khoa, chiếm 3% đến 7% bướu thận (Morra và Das, 1993). Nam giới có tỉ lệ mắc bệnh nhiều gấp đôi nữ (2 : 1), bệnh thường xuất hiện sau 50 tuổi.
Oncocytoma thận thướng có một bao xơ bọc bên ngoài, ít khi xâm lấn bao thận, các đài bể thận hay mô quanh thận. bướu thường có màu vàng hay màu nâu nhạt, trung tâm có sẹo hình sao, và không có mô hoại tử. Oncocytoma ít khi xuất hiện trên cả hai thận.
Về mô học, oncocytoma biệt hóa bao gồm các tế bào biểu mô to, dồng đều, với bào tương ư eosin. Oncocytoma có nguồn gốc từ các ống thận xa, tương tự như chromophobe RCC, và có thể nằm trong hội chứng di truyền Birt-Hogg-Dube. Tuy nhiên, không có bằng chứng cho thấy oncocytoma chuyển thành ác tính.
Chẩn đoán dựa vào lâm sàng, bệnh nhân có biểu hiện đau vùng thắt lưng và tiểu máu khoảng 20% trường hợp. Nếu nghi ngờ Oncocytoma trước mổ, có thể sinh thiết bướu qua da nếu bướu ở vị trí thuận lợi. Cắt lạnh bướu không đáng tin cậy phân biệt oncocytoma và RCC, do đó không nên sử dụng để hướng dẫn phẫu thuật.
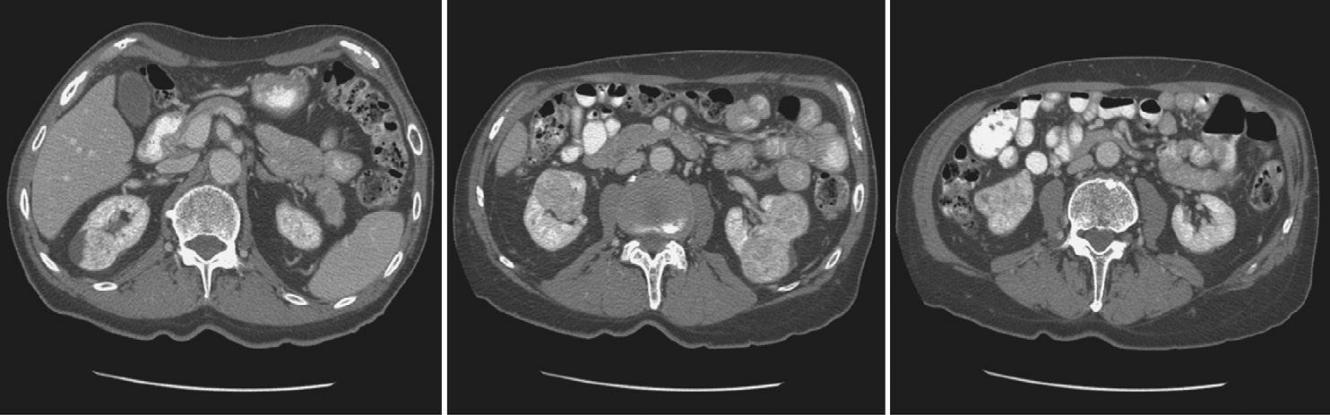
Hình 3. CT scan của bệnh nhân có oncocytoma thận 2 bên (Copyright 2009, S.F. Matin.)
BƯỚU CƠ MỠ MẠCH MÁU (ANGIOMYOLIPOMA)
Bướu mỡ – cơ – mạch (AML) thận là một khối bướu lành tính bao gồm mạch máu, các tế bào cơ trơn và tế bào mỡ. Mô mỡ chiếm tới 80% khối lượng. Phần lớn mô mỡ thuộc nhóm trưởng thành nên có trị số hấp thu âm tính trên chụp cắt lớp vi tính.
Bướu AML thận được xác định đầu tiên bởi Fischer 1911, tên hiện tại của nó đã được đưa ra bởi Morgan năm 1951.
Khác với các loại bướu xuất hiện lẻ tẻ, thể xơ củ (tuberous sclerosis) được Bourneville mô tả năm 1880, bao gồm các triệu chứng chậm phát triển trí tuệ, động kinh, bướu tuyến bã đậu ở mặt và bướu AML thận.
– Về phân loại:
AML là các khối bướu bao gồm những tế bào thượng bì ngoại vi mạch, nghĩa là các tế bào tìm thấy quanh các mạch máu nhỏ dính hoặc đi kèm với các tế bào biểu mô. Khối bướu loại này được biết đến như là PEComa, chính là loại khối bướu nhu mô mạc treo có liên quan đến các tế bào hình thành nên mô liên kết, hệ lympho và tim mạch.
Bướu AML thận từng được coi là một Hamartoma (các khối bướu lành tính bao gồm các tế bào nằm đúng vị trí nhưng hình thành các khối bướu do bị rối loạn tổ chức), hay Choristoma (là các khối bướu lành tính gồm các tế bào bình thường trong một vị trí khác thường).
-
- Có hai loại thể bệnh:
- Thể xơ củ chiếm 20% các AML thận, ở 1 thận hay 2 thận, thường hay phát triển to và gây chảy máu.
- Loại bướu xuất hiện lẻ tẻ, chiếm 80% các AML thận, có xu hướng xuất hiện muộn hơn ở người trưởng thành hoặc ở phụ nữ tuổi trung niên và ít gây biến chứng hơn.
- Có nhiều thụ thể của progesteron và estrogen được tìm thấy ở nhân tế bào cơ trơn của bướu.
- Trong phức hợp xơ củ có 2 gen được tìm thấy là gen TSCl ở nhiễm sắc thể 9 và gen TSC2 ở nhiễm sắc thể 16, có sản xuất chất tuberin. Di truyền theo kiểu autosôm trội, nhưng lại xuất hiện bất thưòng, có thể là do các gen này là gen ức chế bướu.
- Có hai loại thể bệnh:
Đặc điểm lâm sàng:
Tình huống phát hiện bướu thận là phần lớn phát hiện tình cờ bằng siêu âm vì bệnh nhân đi khám vì triệu chứng tiết niệu hay bệnh khác. Khi chẩn đoán một trường hợp bướu thận, đầu tiên nên nghĩ đến RCC.
Tương tự như ung thư tế bào thận (RCC), hầu hết các bướu AML thận được chẩn đoán một cách tình cờ.
Bệnh nhân đến khám thường là nữ, độ tuổi 40, có những triệu chứng sau:
-
-
- Đau bụng và thắt lưng (80%)
- Bướu thận to(50%),
- Tiểu ra máu (25%),
- Xuất huyết sau phúc mạc (30%)
- Tăng huyết áp (20%),
- Thiếu máu (20%),
- Suy thận (5%),
- Nhiễm khuẩn đường tiết niệu (5%).
- Khi có hội chứng xơ cũ, bướu AML xuất hiện ở 1 hay 2 thận gây suy thận nếu bướu phát triển quá to.
-
Bướu AML thận nhỏ hơn 4cm thườngđược theo dỏi dè dặt, tuy nhiên bướu AMLlớn hơn 4cm có triệu chứng trong khoảng 82% các trường hợp và đòi hỏi can thiệp. Vấn đề thường gặp là đau bụng, sờ thấy khối bướu và chứng phình vỡ động mạchtự phát.
Triệu chứng của bướu AML thận xuất hiện khi bướu lớn, nhưng tập trung nhiều khi bướu > 4 cm. Có 82% bệnh nhân có bướu > 4 cm có triệu chứng, với 9% trường hợp sốc do xuất huyết bướu. Ngược lại, bệnh nhân có bướu nhỏ chỉ có 23 % là có triệu chứng.
Có thể sờ thấy khối bướu ở bụng khi khối bướu đã quá lớn. 87% có triệu chứng xuất huyết trong bướu hoặc xuất huyết sau phúc mạc lớn, trong đó xuất huyết sau phúc mạc là biến chứng quan trọng nhất của bướu AML thận chiếm 10 % bệnh nhân.
Nguyên nhân phổ biến nhất của xuất huyết sau phúc mạc tự phátlà bướu AML thận, tiếp theo là RCC. Trong giai đoạn mang thai sẽ làm gia tăng nguy cơ xuất huyết từ bướu AML thận.
Nếu mạch máu bị dãn rộng trong bướu AML thận vỡ ra, dẫn đến hậu quả xuất huyết vào khoang sau phúc mạc lớn, gây đau đột ngột kèm theo buồn nôn và nôn ói. Khi bệnh nhân đến nhập viện vào khoa cấp cứu thì có đến 20% trường hợp bị sốc. Chẩn đoán cận lâm sàng
- Siêu âm bụng tổng quát:
Phân biệt bướu AML thận và bướu RCC thận trên siêu âm:
-
- Chẩn đoán bướu AML thận dựa vào siêu âm có thể thường nhầm lẫn với bướu RCC thận lên đến 12% và tăng đến hơn 30% khi bướu nhỏ (<3 cm).
- So sánh các đặc điểm siêu âm của AML và RCC cho thấy một vành giảm cản âm và / hoặc trong nang gợi ý nhiều RCC, cản âm dày có bóng lưng trong 33% của AML và không có trong RCC.
- Tổn thương thận nhỏ (<3 cm) bướu AML thận có thể có bóng lưng (21%), nhưng không có trong bướu RCC thận. Bướu thận có cản âm dày với bóng lưng gợi ý nhiều đến AML, nhưng không phải là phương pháp có độ nhạy cao.
- Bướu AML thận có ít mỡ có các cản âm cùng đậm độ, đồng nhất trong bướu AML thận và không có trong bướu RCC thận.
- CT scan bụng cản quang và không cản quang:
- Giúp phát hiện ra bướu thận hoặc các tổn thương nghi ngờ là bướu. Chụp CT bụng không cản quang trước, sau đó bơm thuốc cản quang, phim chụp sau 1 phút sẽ thấy rõ nhu mô thận, sau đó 10 phút chụp 1 phim.
- CT cho kết quả mô tả chi tiết và nhanh chóng cũng như cho phép đo kích thước chính xác. Song, nếu có tiêm thuốc cản quang để mô tả kỹ hơn cho tổn thương của bướu thì sẽ có nguy cơ nguy hiểm và gây độc cho thận.
- CT có thể đánh giá sự xâm lấn vùng của bướu và xâm lấn mạch máu (hay có hiện diện của chồi bướu trong tĩnh mạch), khi có hiện diện của thành phần mỡ
trong bướu có thể là bướu AML thận trong những trường hợp khó chẩn đoán bằng siêu âm.
-
- CT cũng cho phép phát hiện sự bất thường của thận đối diện hay không.
- Chụp cộng hưởng từ (MRI):
MRI an toàn hơn CT nhưng nhiều bệnh nhân (đặc biệt trên các bệnh nhân có rối loạn hành vi và trên các bệnh nhân có tuberous sclerosis) đòi hỏi phải dùng thuốc an thần hoặc gây mê và vì thế scan không thể thực hiện nhanh chóng được.
MRI cũng được chỉ định khi nghi ngờ có chồi bướu trong tĩnh mạch, xác định xem nó ăn lan tới đâu (tĩnh mạch chủ hay tới tâm nhĩ phải), MRI cũng có thể thay thế CT để chẩn đoán và đánh giá giai đoạn bướu khi không thể thực hiện CT như dị ứng thuốc, suy thận.
Theo dõi và điều trị bướu AML thận
Hầu hết AML thận không phát triển thêm. Tuy nhiên, một số phát triển chậm, thường với tỉ lệ 5% mỗi năm tương đương 0,088 cm mỗi năm.
Một số bướu AML thận, đặc biệt là bướu lớn hơn 4 cm, có thể gây chảy máu nhiều và trầm trọng, có thể đe dọa tính mạng. Như vậy, dù bướu AML thận là lành tính, một số bướu có thể được chỉ định theo dõi hình ảnh học ngay cả khi không có triệu chứng.
Các điều trị bảo tồn thận với bướu AML thận nhỏ cần can thiệp
-
- Tắc mạch chọn lọc
- Cắt thận bán phần
- Thuyên tắc mạch chọn lọc lựa chọn cho các bệnh nhân có thể ảnh hưởng chức năng thận trong tương lai như:
- Bướu AML thận trong TSC bị bướu 2 bên
- Suy thận đã có từ trước
- Bướu AML thận lớn trên thận đơn độc
- Bệnh cấp cứu và có khả năng xuất huyết đe dọa tính mạng yêu cầu cắt thận Mặc dù, tắc mạch chọn lọc ghi nhận thành công lâu dài trong các trường hợp nhưng
có một tỉ lệ lớn bệnh nhân phải trải qua tắc mạch lặp đi lặp lại khi có xuất huyết bướu tái phát, đôi khi cần cắt thận bán phần.
Phương pháp điều trị xâm lấnnhư cắt bỏ khối bướu bằng đốt nhiệt cũng đã được sử dụng để điều trị bướu AML thận, nhưng thời gian theo dõi vẫn còn ngắn, đánh giá thành công vẫn còn kém và thời gian để tiếp tục theo dõi bằnghình ảnh học là không rõ. Phương pháp điều trị xâm lấn này có thể có vai trò để điều trị bệnh nhân bướu AML thận có TSC hoặc bệnh nhân lớn tuổi với các bệnh đi kèm cần điều trị và không
điều trị tắc mạch được.
- Chỉ định chính để can thiệp phẫu thuật điều trị, bao gồm:
- Có triệu chứng đau
- Xuất huyết khối bướu sau phúc mạc
- Nghi ngờ ác tính.
Theo Hướng dẫn điều trị của Hội niệu khoa Châu Âu 2014 thì bướu AML thận xem xét điều trị (phẫu thuật, đốt nhiệt, tắc mạch chọn lọc) trong các trường hợp:
-
- Bướu lớn (ngưỡng đề nghị can thiệp không rõ, thường kích thước bướu >4 cm)
- Phụ nữ tuổi sinh đẻ dự định có thai
- Bệnh nhân đang theo dõi bướu AML và không có điều kiện can thiệp cấp cứu đầy đủ.
Đối với bướu AML thận nhỏ hơn 4 cm và không có triệu chứng, theo dõi với siêu âm mỗi 12 tháng.
Nếu khối bướu nhỏ hơn 4 cm và người bệnh có triệu chứng, có thể chọn kỹ thuật điều trị bằng làm tắc mạch chọn lọc hoặc cắt thận bán phần nhưng theo dõi thường được lựa chọn trong thực hành lâm sàng.
Đối với những khối bướu lớn ở những bệnh nhân không có triệu chứng, theo dõi với CT hoặc siêu âm bụng tổng quát được khuyến khích.
Bệnh nhân có triệu chứng với những khối bướu lớn hơn 4 cm, đặc biệt là những người có khối bướu đã bị xuất huyết, điều trị tắc mạch chọn lọc hoặc cắt thận bán phần thường được khuyến cáo.
BƯỚU THẬN DẠNG NANG VÀ BƯỚU HỖN HỢP MÔ ĐỆM/BIỂU MÔ
(CYSTIC NEPHROMA AND MIXED EPITHELIAL/STROMAL TUMOR)
Mặc dù được WHO phân thành 2 loại bướu riêng biệt, bướu thận dạng nang và bướu hỗn hợp mô đệm/biểu mô là bướu lành tính có lâm sàng và hình ảnh học chồng chéo nhau. Các hormon giới tính có thể đóng vai trò trong sinh bệnh học của các tổn thương trên.
Bướu thận dạng nang
Bướu thận dạng nang là một tổn thương thận, với đỉnh tuổi 2-3 tuổi (chủ yếu ở nam giới), và 40-50 tuổi (nữ gấp 8 lần nam).
Khó phân biệt trên hình ảnh học giữa bướu thận dạng nang với bướu Wilms ở trẻ em và RCC ở người lớn (Vujanic và cộng sự, 2000).
Hầu hết bướu thận dạng nang trẻ em được cắt thận triệt để, trong khi ở người lớn cắt bán phần thận.
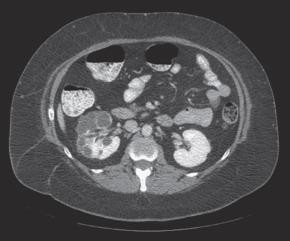
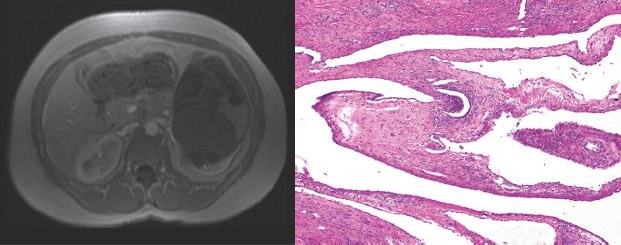
A B C
Hình 5. CT (hình A) và MRI (hình B) không giúp phân biệt với RCC hoặc bướu Wilms dạng nang. Hình C: các khoảng không gian trong nang được lót bởi biểu mô phẳng.
Bướu mô hỗn hợp đệm/biểu mô (MEST):
MEST là một bướu thận lành tính hiếm gặp với thành phần hỗn hợp biểu mô và trung mô. Tương tự như bướu thận dạng nang, MEST ưu thế ở nữ, khoảng 40 tuổi. Đa số bệnh nhân nữ có tiền căn sử dụng liệu pháp thay thế estrogen, và bệnh nhân nam duy nhất bị MEST do sử dụng kháng androgen điều trị ung thư tuyến tiền liệt (Adsay và cộng sự, 2000).
Hình ảnh của MEST là một khối nang thận phức tạp, thuộc Bosnia loại III IV, không thể phân biệt với RCC (Adsay và cộng sự, 2000).
Chẩn đoán MEST trước phẫu thuật cần được xem xét với phụ nữ quanh mãn kinh được điều trị nội tiết tố; Tuy nhiên, vì hình ảnh học không đáng tin cậy để phân biệt với RCC, nên phương pháp thích hợp với bệnh nhân là phẫu thuật.

A B C
Hình 6. Hình A: CT scan không thể giúp phân biệt với RCC. Hình B: hình đại thể cắt một phần thận thấy nhiều nang kích thước khác nhau được ngăn cách bởi các vách dày màu trắng. Hình C: các nang được lót bởi các tế bào đầu đinh và mô đệm tế bào hình thoi.
Bướu cơ trơn:
Bướu cơ trơn rất hiếm, có thể phát sinh từ các tế bào cơ trơn bất cứ nơi nào dọc theo đường sinh dục (Tamboli và cộng sự, 2000). Ở thận thường phát sinh từ bao thận, nhưng bể thận và tĩnh mạch thận cũng có thể gặp (Wells và cộng sự, 1981; Steiner et al, 1990; O’Brien và cộng sự, 1992; Rao và cộng sự, 2001). Bướu cơ trơn chiếm khoảng 4,2% đến 5,2% khi khám nghiệm tử thi, nhưng chỉ chiếm khoảng 1,5% của tất cả các khối bướu lành tính thận điều trị phẫu thuật (Romero và cộng sự, 2005).
Khó phân biệt bướu cơ trơn và RCC trên hình ảnh học (Steiner et al, 1990; Derchi et al, 2008). Bướu lớn có thể phải cần cắt thận, nhưng với bướu ngoại biên nhỏ chỉ cần cắt một phần thận.
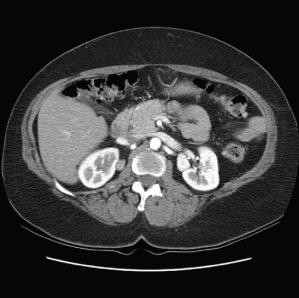
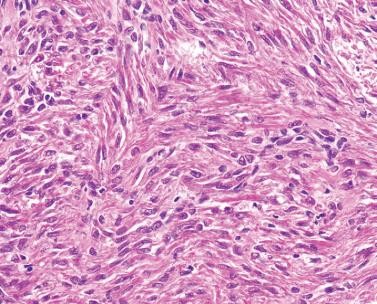

A B C
Hình 7. Hình A: CT scan cho thấy có một khối ở thận bắt nguồn từ bao thận. Hình B: Tế bào hình thoi đồng dạng, nhân hình điếu xì gà mỏng không có dị dạng nhân. Hình C: Hóa mô miễn dịch dương mạnh với SMA trong tế bào cơ trơn. Các ống thận bình thường bên phải âm tính với SMA.
Các bướu thận lành tính khác:
Các khối bướu lành tính hiếm có nguồn gốc từ các thành phần trung mô khác nhau của thận đã được mô tả bao gồm: bướu xơ, bướu mỡ, bướu bạch huyết, và bướu mạch máu (Ligato và cộng sự, 1999; Tamboli và cộng sự, 2000).
Hình ảnh học hiện tại không giúp phân biệt biệt các bướu lành tính với tổn thương thận ác tính, cần phải phẫu thuật làm giải phẫu bệnh để xác định chẩn đoán.
Bướu tiết renin là bướu lành tính của phức hợp cạnh cầu thận, là một nguyên nhân quan trọng nhưng hiếm gặp của tăng huyết áp thứ phát và hạ kali máu. Biểu hiện lâm sàng chủ yếu là tăng tiết renin: tăng huyết áp, hạ kali máu và các triệu chứng liên quan như đa niệu, đau cơ và đau đầu (Schonfeld et al, 1991; Rubenstein và cộng sự, 2002). Chẩn đoán dựa vào hội chứng cường aldosteron thứ phát, được xác định bằng định lượng renin trong tĩnh mạch thận. Điều trị bằng cách phẫu thuật cắt bướu rất có hiệu quả.

YKHOA247.com thành lập với mục đích chia sẻ kiến thức Y Khoa.
Mọi thông tin trên trang web chỉ mang tính chất tham khảo, bạn đọc không nên tự chẩn đoán và điều trị cho mình.
